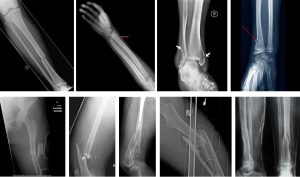
Остеосинтез або металоостеосинтез (МОС) у лікуванні переломів кісток
- – Що таке остеосинтез?
- – Які види остеосинтезу бувають?
- – Показання та протипоказання.
- – У яких випадках застосовують той чи інший метод остеосинтезу?
- – Сучасні методи остеосинтезу та погляд у майбутнє.Відділення травматології та ортопедії дорослих ДУ НІТО НАМНУ

В Україні остеоартроз є найпоширенішим захворюванням суглобів. Так, за даними державної статистичної звітності за 2014 рік, його поширеність становила 3140 випадків на 100 тис. населення, захворюваність – 460 випадків на 100 тис. населення. У більшості країн частота та поширеність асептичного некрозу (АН) вивчені недостатньо. За даними різних авторів, він зустрічається у 1,4-4,7% пацієнтів із патологією кульшового суглоба. У США щорічно реєструється близько 15 тис. нових випадків АН, понад 10% від загальної кількості ендопротезувань кульшового суглоба спричинені його наслідками. У Японії щороку діагностується 1,5-3,3 тис. випадків асептичного некрозу стегна, із них 34,7% викликані вживанням кортикостероїдів, 21,8% – зловживанням алкоголем та 37,1% спричинені ідіопатичними механізмами…
Ендопротезування кульшового та колінного суглобів, без сумніву, займає лідируючі позиції в оперативному лікуванні остеоартрозу та АН кульшового й колінного суглобів. Число зазначених оперативних втручань зростає щороку, й у найближче десятиліття ця тенденція зберігатиметься. Так, за даними Американської академії хірургів-ортопедів та страхової компанії NerdWallett Health, медична система США щороку витрачає близько 6 млрд доларів на ендопротезування кульшового та колінного суглобів. За даними Journal of Bone & Joint Surgery, у період із 1971 по 2003 рік кількість випадків ендопротезування колінного суглоба у світі зросло на 400%, кульшового – на 55%. За прогнозами, у 2030 році кількість первинних ендопротезувань колінного суглоба сягне 3,48 млн на рік, а ревізійних ендопротезувань колінного та кульшового суглобів зросте відповідно на 600% та 137% порівняно з 2005 роком. Така тенденція спонукає до пошуку альтернативних методик лікування з метою стримування подальшого інтенсивного росту кількості ендопротезувань та досягнення позитивного економічного й соціального ефекту. Однією з таких альтернатив стають технології регенеративної медицини, зокрема застосування клітинної терапії у пацієнтів з остеоартрозом та АН кульшового й колінного суглобів (Centeno C., 2018-2019).
Етіологія захворювання до цього часу остаточно не вивчена, але в патогенезі з’явилися цікаві нові дані. На сьогодні велика увага приділяється змінам остеохондрального переходу, а саме: зміна фаз перевантаження та відновлення остеохондрального переходу призводить до запуску механізмів, кінцевими процесами яких є екструзія мінералів високої щільності у гіаліновий хрящ та утворення остеофітів із подальшим прогресуванням остеоартрозу (Boyde A., 2021).
Етіологію АН можна розділити на такі групи:
- травматичні причини (переломи ділянки суглоба, травматичні дислокації);
- нетравматичні причини (прийом кортикостероїдів, зловживання алкоголем, вживання наркотичних речовин, вплив токсинів, радіоактивного випромінення, жирова емболія, коагулопатії, серпоподібноклітинна анемія, хвороба Гоше, кесонна хвороба).
Патогенетичні механізми АН різняться залежно від етіологічних чинників. Нетравматичний АН характеризується додатковою гіпертрофією адипоцитів як первинної ланки патогенезу, а далі механізм однаковий, незалежно від етіологічних чинників: порушення кровопостачання епіфізу призводить до критичної ішемії й некрозу кістки з наступним запаленням, резорбцією та руйнуванням кісткової тканини.
Відомо, що для регенерації тканин опорно-рухового апарату необхідні чотири компоненти:
- клітинний (тромбоцити, фібробласти, мезенхімальні стовбурові клітини, хондроцити та остеобласти);
- морфогенетичний (фактори росту);
- провідний (scaffold);
- механічний.
Офіційні рекомендації щодо лікування остеоартрозу та АН залежно від тяжкості перебігу передбачають наступне: фізіотерапія, розвантаження суглоба, зниження ваги, ортезування, лікувальна фізкультура. На більш пізніх етапах: фармакологічні інтервенції для зменшення больового синдрому (нестероїдні протизапальні препарати, хондропротектори, віско-суплементація, ін’єкції стероїдів). У найбільш тяжких випадках – хірургічні втручання (артроскопічні техніки, тунелізація, тотальне ендопротезування суглобів).
Регенеративні технології наразі вважаються альтернативними методами лікування, хоча їх застосування забезпечує процес відновлення тканин усіма необхідними складовими.
Співробітниками ДУ «Інститут травматології та ортопедії НАМН України» була розроблена робоча класифікація біотехнологічних продуктів (Страфун С.С., Голюк Є.Л.):
1-ша лінія – засоби, які при введенні в ушкоджену ділянку стимулюють виділення організмом власних факторів росту;
2-га лінія – аутологічні тромбоконцентрати:
А) з малою (<1 млн клітин на 1 мкл) клітинністю (збіднена на тромбоцити плазма, концентрована плазма);
Б) аутологічні тромбоконцентрати зі значною (>1 млн клітин на 1 мкл) клітинністю (збагачена тромбоцитами плазма, низьколейкоцитарна та збагачена лейкоцитами, гіперконцентрат тромбоцитів, збагачений тромбоцитами фібрин);
В) кріолізат тромбоцитів;
3-тя лінія – аутологічні концентрати жирової клітковини та КМ:
А) концентрати жиру та КМ, отримані шляхом механічної обробки (мікрофрагментований жир, концентрат аспірату КМ),
Б) концентрати жиру та КМ, отримані шляхом механічної та біотехнологічної обробки (стромально-васкулярна фракція жирової клітковини, мононуклеарна фракція аспірату КМ) та їхні похідні;
4-та лінія – біотехнологічні продукти, отримані шляхом культивування клітин або іншої високотехнологічної обробки;
5-та лінія – фармакологічні препарати на основі цитокінів, стовбурових клітин, генно-інженерні препарати.
Ця класифікація передбачає, що біотехнологічний продукт попередньої лінії може бути скафолдом для продукту наступної лінії. Наприклад, збагачена тромбоцитами плазма при комбінованому застосуванні буде скафолдом для концентратів, що містять мезенхімальні стовбурові клітини (МСК).
Найбільш поширеними в ортопедичній та травматологічній практиці, у тому числі при лікуванні остеоартрозу та АН, є процедури клітинної терапії «одного дня» за допомогою аутологічних біотехнологічних продуктів.
Щодо тактики застосування регенеративних технологій, то при остеоартрозі та АН завжди починають з ін’єкції тромбоконцентратів. Чим більш тривалим є курс клітинної терапії, тим більш повним та тривалим буде подальший позитивний клінічний ефект. Залежно від діагнозу та перебігу захворювання спікер рекомендував від двох до шести ін’єкцій тромбоконцентратів (1 раз на 1-2 тижні) як підготовчий етап для введення концентратів, що містять МСК. При АН, у разі якщо пацієнт потребує швидкого проведення оперативного втручання, ін’єкційну терапію тромбоконцентратами проводять у післяопераційному періоді. Вводити МСК необхідно за допомогою ультразвукової навігації або навігації на основі електронно-оптичного перетворювача.
Вибір тактики застосування регенеративної ін’єкційної терапії при остеоартрозі значною мірою залежить від його фенотипу, яких на сьогодні в літературі зустрічається шість. Найбільш складним у прогностичному плані щодо застосування регенеративних технологій є пацієнти з переважанням механічного фенотипу, у яких превалюють порушення біомеханіки суглоба (обмеження рухів, деформації, значні зміни у геометрії суглобів).
Доповідач навів результати дослідження, у якому оцінювали зміну якості життя пацієнтів із різними стадіями остеоартрозу після застосування регенеративних технологій (Goliuk Ye. et al., 2020). Так, при 1-й стадії протягом першого року після введення аутологічних тромбоконцентратів відмічалося постійне зниження больового синдрому та покращення показників якості життя. У пацієнтів із 2-ю стадією спостерігались подібні результати, але на цій стадії рекомендовано внутрішньосуглобове введення препаратів комбінувати з регіонарними методиками (капсула та бокові зв’язки). При 3-й стадії через 3 міс після лікування спостерігалась тенденція до погіршення якості життя й відновлення больового синдрому, тому у перші 3 міс після завершення курсу лікування тромбоконцентратами рекомендовано введення МСК.
Для вибору відповідної тактики застосування регенеративних технологій при АН використовують класифікацію Японського дослідницького комітету (JIC) та керуються стадією процесу (преколаптоїдна/постколаптоїдна):
- При типі А ризик руйнування головки відсутній – рекомендована внутрішньосуглобова регенеративна ін’єкційна терапія тромбоконцентратами з подальшим внутрішньосуглобовим введенням МСК.
- При типі В ризик руйнування складає близько 10% – рекомендовано попереднє введення тромбоконцентратів із подальшим внутрішньокістковим введенням (тунелізацією) МСК у зону некрозу.
- При типі С1 ризик руйнування складає близько 30% – рекомендовано попереднє введення тромбоконцентратів з розвантаженням суглоба та подальше внутрішньокісткове введення (тунелізація) МСК у зону некрозу.
- При типі С2 ризик руйнування складає близько 70% – рекомендовано до- та післяопераційне введення тромбоконцентратів із внутрішньокістковим (тунелізацією) та внутрішньосуглобовим введенням МСК.
Що таке остеосинтез?
Як пише Вікіпедія – Остеосинтез — (др.-греч. ὀστέον — кістка; σύνθεσις — зчленування, з’єднанняе) хірургічна репозиція (співставлення) кісткових уламків за допомогою різних фіксуючих конструкцій, що забезпечують тривале усунення їхньої рухливості. Мета остеосинтезу – забезпечення стабільної фіксації уламків у правильному положенні зі збереженням функціональної осі сегмента, стабілізація зони перелому до повного зрощення. У свою чергу більш розширена назва металоостеосинтез (МОС) передбачає використання як фіксаторів імплантів з різних сплавів металів або комбінації металів і полімерів, які мають біологічну, хімічну і фізичну інертність і не вступають у взаємодію з організмом. Як матеріали використовуються різні сплави сталей, титану та комбінації цих матеріалів з полімерами або керамікою як у випадку з ендопротезами.
Металоостеосинтез (МОС переломів) є одним з основних методів при лікуванні нестабільних переломів довгих трубчастих кісток, а часто єдино можливим (крім ендопротезування пошкодженого суглоба) особливо при внутрішньосуглобових переломах з порушенням цілісності суглобової поверхні, багатоуламкових переломах з великим зміщенням та великих кісткових дефектах. Сучасний остеосинтез почав своє формування наприкінці 1800-х на початку 1900-х років. Але деякі знахідки археологів підтверджують, що внутрішньокісткові або накісткові імпланти застосовувалися ще в стародавньому Єгипті, Китаї та Індії.
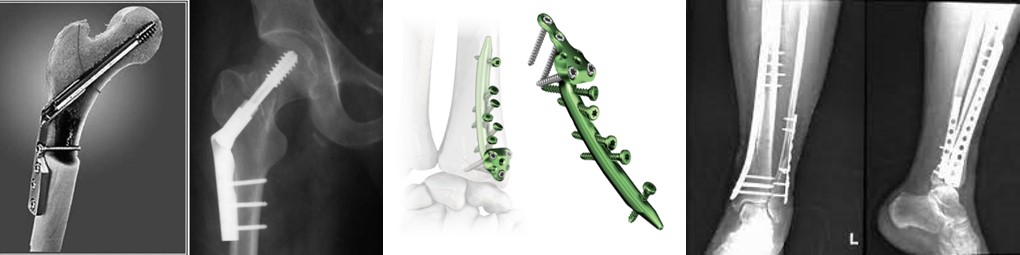
Які види остеосинтезу бувають?
Остеосинтез ділять на кілька видів:
Зовнішній (чрезезкістковий остеосинтез) – втручання в зону перелому не здійснюється, для фіксації застосовують апарати Ілізарова, Костюка, Волкова-Оганесяна, АВФ (апарат зовнішньої фіксації) та ін., спиці та стрижні яких проводяться через кістки вище та нижче області перелому.

Різновиди апаратів зовнішньої фіксації
Погружний (внутрішній) остеосинтез – фіксатор вводиться в зону перелому, погружна техніка поділяється на три методики: черезкісткову, накісткову та внутрішньокісткову.
Погружний черезкістковий – фіксаторами виступають гвинти або спиці. Їх вводять у перелом поперечно, поздовжньо чи під кутом. Методика показана при спіралеподібних переломах, переломах фаланг пальців, переломах кістки п’яти, надколінка, виростків, синдесмозу, кісточок і т. д.
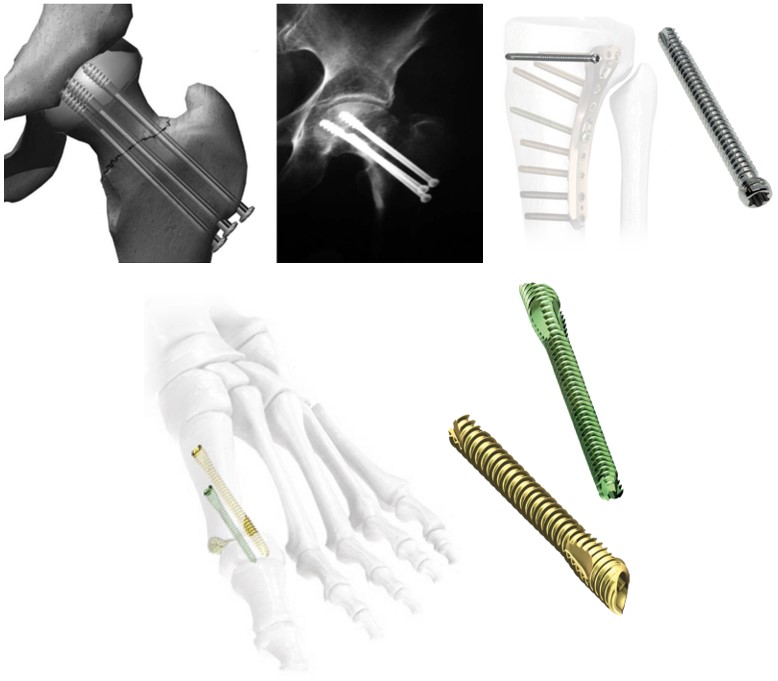
Гвинти для черезкісткового остеосинтезу переломів кісток
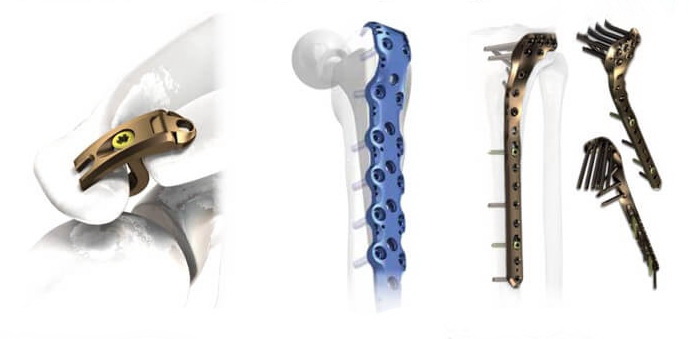
Погружний накістковий – застосовують у більшості випадків при переломах трубчастих кісток будь-якої локалізації, закриті переломи зі зміщенням без ускладнень (поперечні, уламкові та ін.). Імпланти – металеві пластини, що кріплять до кісток гвинтами. Сучасні пластини, в свою чергу, діляться на безліч видів: малоінвазивні, з мінімальним контактом, блоковані, біфазні тощо.
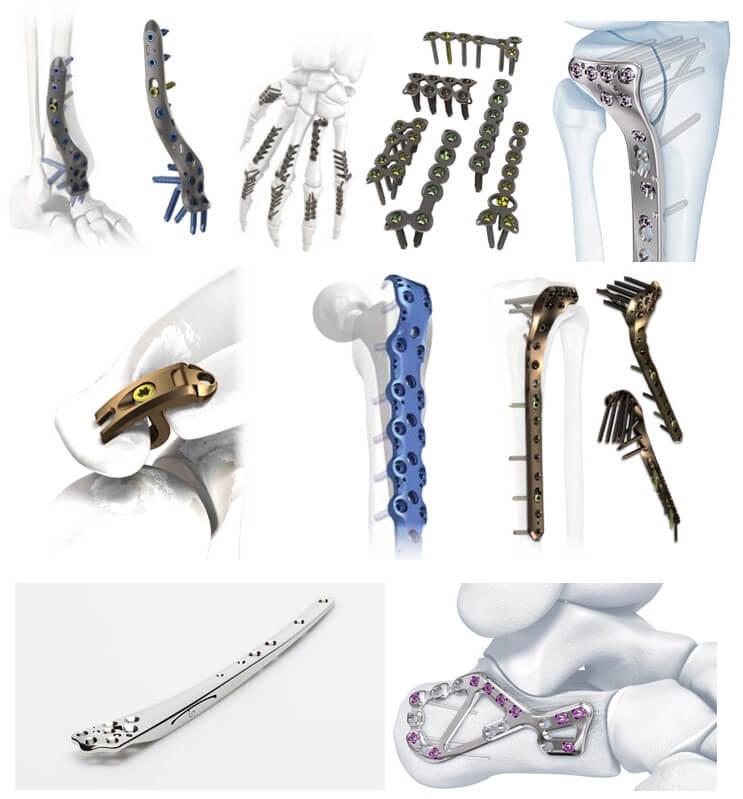
Остеосинтез або металоостеосинтез (МОС) у лікуванні переломів кісток. Пластини для фіксації уламків при переломах різної локалізації
Погружний внутрішньокістковий – застосовують при переломах трубчастих кісток, практично будь-якої локалізації. Операція проводиться з відкритим доступом у зоні перелому чи закритим (без доступу до зони перелому). У першому випадку уламки кісток зіставляють без спеціальних апаратів, лише хірургічним інструментарієм. Закрита техніка передбачає використання направляючого пристрою (навігатора) та введення в кістковомозковий канал металевого або полімерно-металевого стержня. Зазвичай, маніпуляції проходять під контролем рентгенографії або ЕОПа, проте сучасні навігаційні системи дозволяють обходитися без рентгенконтролю під час операції.
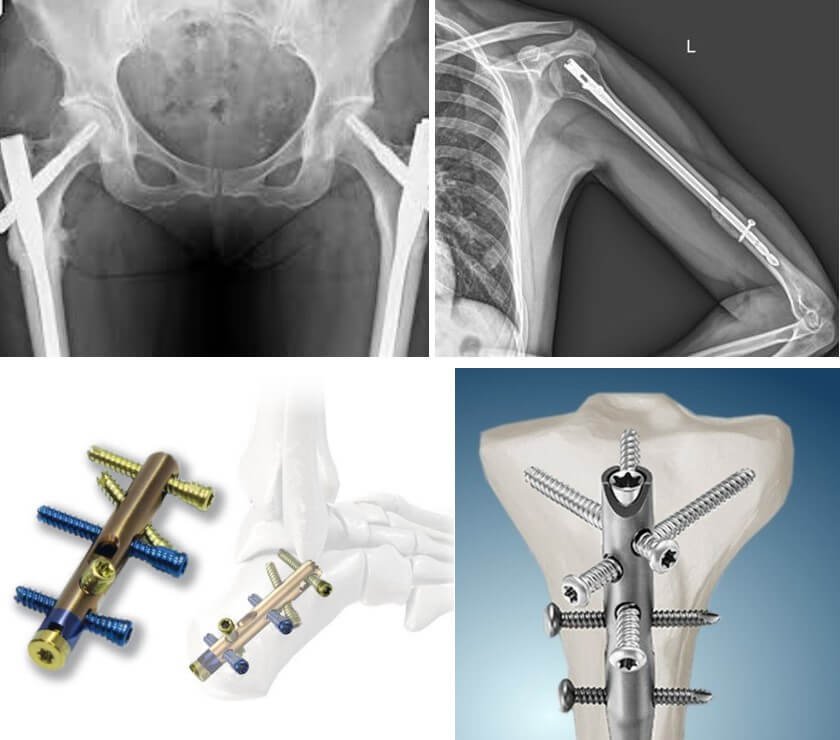
Стержні для інтрамедулярного остеосинтезу
Ще один вид остеосинтезу – залежно від термінів проведення операції. Залежно від часу, що минув з травми до операції, остеосинтез ділиться на 2 типи:
Первинний. У цьому випадку операція МОС проводиться у перші 12 годин після травми.
Відстрочений. Якщо операція проводиться через 12 годин після травми.
Якщо було проведено відстрочений остеосинтез, це означає, що допомога «запізнилася» чи що час втрачено. Який вид операції буде кращим для кожного випадку, вирішує лікар виходячи із загального стану пацієнта, супутніх травм і захворювань, наявності того чи іншого імпланту в операційній і т. д.
Показання та протипоказання. У яких випадках застосовують той чи інший метод остеосинтезу?
Показання
Абсолютними показаннями до остеосинтезу є нестабільні переломи зі значним зміщенням уламків, багатоуламкові переломи, які без репозиції та фіксації не зростаються, наприклад переломи ліктьового відростка та надколінка з розходженням уламків, деякі типи переломів шийки стегнової кістки; внутрішньосуглобові переломи (виростків стегнової і великогомілкової кісток, дистальних метаепіфізів плечової, променевої кісток) переломи, у яких існує небезпека перфорації кістковим уламком шкіри, тобто, перетворення закритого перелому на відкритий; переломи, що супроводжуються інтерпозицією м’яких тканин між уламками або ускладнені ушкодженням магістральної судини чи нерва.
Протипоказання
Абсолютним протипоказанням може лише загальний стан пацієнта. Щоб уникнути додаткової травматизації, застосування наркозу, можливої втрати крові, операцію можуть відкласти до стабілізації загального стану.
Відносними протипоказаннями до того чи іншого методу остеосинтезу можуть бути:
- захворювання крові пов’язані з порушенням її згортання, низький гемоглобін, сепсис
- гострі інфекційні захворювання, гнійні ураження шкіри у місці операційних доступів
- остеопороз та порушення обміну речовин (зміна методів фіксації)
Чітких алгоритмів, які визначають метод фіксації уламків, немає. Є рекомендації та наукові роботи, які доводять перевагу того чи іншого способу при переломах певної локалізації.
Відносні та абсолютні показання у виборі імплантів (у більшості випадків) є тільки для фіксації відкритих та закритих переломів. При відкритих переломах, особливо з ризиком інфікування зони пошкодження, не рекомендують використовувати внутрішньокістковий та кістковий остеосинтез стрижнями та пластинами, в даному випадку використовують АЗФ або інші способи зовнішньої фіксації. Апарати зовнішньої фіксації можуть використовувати як постійний спосіб і вести пацієнта до повного зрощення перелому або використовувати їх як тимчасовий спосіб до загоєння м’яких тканин з наступною заміною способу фіксації на інтрамедулярний стержень або пластину з мінімальним контактом.
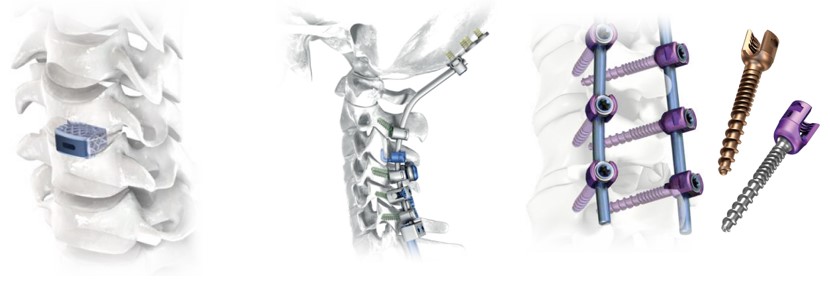
Імпланти для остеосинтезу переломів хребта
Коли потрібно видаляти імпланти після остеосинтезу і чи потрібно це робити?
Пацієнтів завжди цікавить питання, чи обов’язкове видалення імпланту після остеосинтезу – чи можна обійтися без повторної операції, залишивши в організмі штифт, гвинт, пластину чи спицю. У деяких випадках травматологи можуть рекомендувати залишити фіксатори назавжди, проте видалення є обов’язковим у таких випадках:
- – видалення конструкції передбачено методом операції (блоковані штифти та пластини для інтрамедулярного остеосинтезу);
- – інфікування та розвиток гнійного процесу (остеомієліт);
- – молодий вік пацієнта (фіксатор перешкоджає розвитку та зростанню сегмента);
- – незрощений перелом після першої операції (видалення попередньої та встановлення нової конструкції);
- – індивідуальний дискомфорт, викликаний присутністю імплантату в незручному місці (ключиця, лікоть, кісточки, п’ята, кисть …)
- – міграція імплантів
Переваги та недоліки остеосинтезу в лікуванні переломів
До переваг остеосинтезу можна віднести:
- – відновлення цілісності кістки без накладання гіпсу, що сприяє ранній реабілітації та запобігає розвитку контрактур прилеглих суглобів;
- – стабільна фіксація в анатомічно правильному положенні із зіставленням уламків;
- – можливість починати ходити ще до настання повного зрощення перелому (тільки за умов досягнення стабільної фіксації);
- – метод застосовується у разі складних переломів зі зміщенням та вивихом, коли накладення гіпсу малоефективне та шкодить суглобам (позбавляє суглоб рухливості після фіксації та несе ризик розвитку контрактур)
При правильно підібраному способі фіксації, відсутності ускладнень, розпочатій вчасно реабілітації повернутись до звичного способу життя можна через 3-6 місяців залежно від локалізації перелому та вибору способу остеосинтезу.
Недоліки:
- – вартість імплантів. Деякі фіксатори можуть коштувати десятки тисяч гривень.
- – необхідність видаляти після зрощення перелому (повторна операція)
- – індивідуальна непереносимість (реакція на метал)
Ризики ускладнень:
- – приєднання інфекції,
- – поломка фіксатора через заводський дефект, надмірне навантаження, повторну травму (падіння на кінцівку з фіксатором)
- – незрощення переломів через неправильний вибір імпланту, неадекватну фіксацію, порушення обміну речовин (остеопороз) або неправильну реабілітацію
- – міграція імплантів
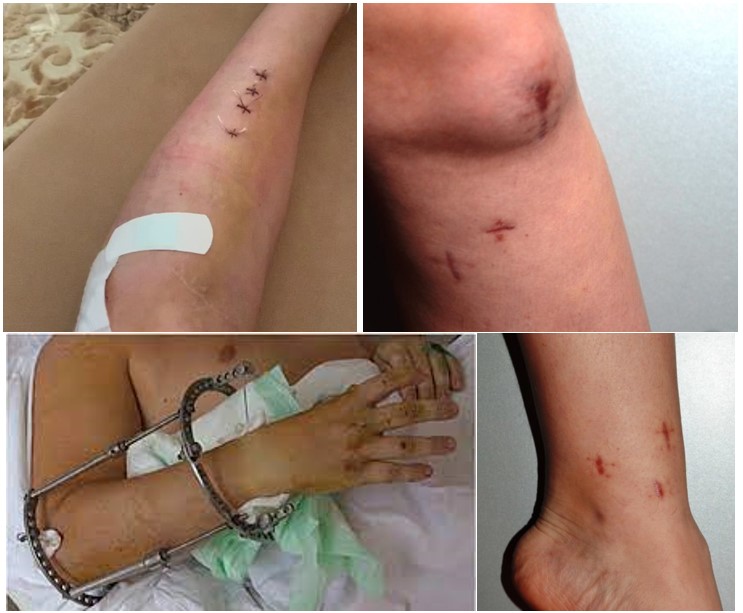
Зовнішній вигляд при різних способах остеосинтезу (пластини, стрижні, гвинти, АЗФ)
Останнім досягненням в області накісткового остеосинтезу стали пластини з кутовою стабільністю, а тепер ще й поліаксіальною стабільністю (LCP). Крім різьблення на гвинті, за допомогою якого він вкручується в кістку і фіксується в ній, є різьблення в отворах пластини і в гвинтовій головці, за рахунок чого головки кожного гвинта міцно фіксуються в пластині що запобігає можливості міграції гвинта. Такий спосіб фіксації гвинтів у пластині значно збільшує стабільність остеосинтезу.
Сучасні методи остеосинтезу та погляд у майбутнє

Створені пластини з кутовою стабільністю для кожного з сегментів усіх довгих трубчастих кісток, що мають форму яка відповідає формі та поверхні сегмента. Наявність анатомічних пластин надає значну допомогу при репозиції перелому.

Ще один сучасний винахід, який зараз проходить клінічні випробування в реальних умовах, біфазна пластина

Система перипротезних проксимальних стегнових пластин LCP зі змінним кутом 3,5/4,5 виготовляється з нержавіючої сталі. Зображені такі конфігурації пластин: проксимальна стегнова пластина з кільцевою додатковою пластиною для великого вертлюга, додаткова блокуюча пластина зі змінним кутом, додаткова обвідна пластина для дистальної частини стегна.
Інтрамедулярні стержні з поліаксіальною стабільністю в 3-х площинах, анатомічні для різних сегментів з навігаційними системами, максимально спрощую імплантацію навіть без наявності ЕОПа або рентгена в операційній.
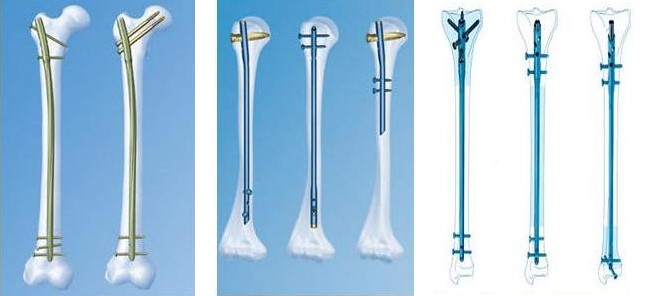
Сучасна система інтрамедулярного остеосинтезу великогомілкової кістки з навігатором
Хотілося б відзначити перспективні розробки у галузі біодеградуючих матеріалів. Імпланти з таких матеріалів не потребують видалення. На жаль, у клінічній практиці такі фіксатори поки що не набули широкого застосування.
Підбиваючи підсумки
У більшості випадків при переломах остеосинтез є єдиним методом лікування, який у стислий термін допомагає пацієнтові повернутися до звичного способу життя, уникнути контрактур та інших ускладнень від застосування гіпсових пов’язок або тривалого перебування на скелетному витягуванні. Остеосинтез може застосовуватися практично на будь-якій кістці або сегменті від кінчиків пальців на руках до хребта та кінчиків пальців на ногах. Величезна різноманітність фіксаторів допомагає лікареві зробити оптимальний вибір при фіксації перелому. Можливі недоліки та ускладнення з кожним новим імплантом стають все незначнішими та рідшими. Біоінертні матеріали допомагають уникнути непереносимості та алергічних реакцій практично у будь-якого пацієнта, а нові сплави дозволяють здійснювати дозовані навантаження на пошкоджені кінцівки з перших днів після операції.
Про нас
Відділення травматології та ортопедії дорослих ДУ НІТО НАМНУ
На сьогодні, основними напрямками науково-практичної діяльності відділення травматології та ортопедії дорослих є ортопедичне лікування дегенеративно-дистрофічних захворювань суглобів (остеоартроз, асептичний некроз, внутрішньосуглобові переломи та їх наслідки та ін.), всі види артроскопічних втручань на колінному суглобі, коригуючі остеотомії, первинне, ревізійне та індивідуальне ендопротезування кульшового та колінного суглобів, лікування переломів та їх наслідків.
Олег Анатолійович Костогриз - Завідувач відділу травматології та ортопедії дорослих, доктор мед. наук, Заслужений лікар України
Записатися на прийом
Тел:
+38(099)064-82-87
+38(096)064-82-87
E-mail:
arthroclinic.com.ua@gmail.com
Працюємо ...
Пн - Пт: 09.00 -16.00
Сб - Нд: вихідний
Через дію військового стану та ведення бойових дій, всі консультації проводяться за попереднім узгодженням з лікарем. Дякуємо за розуміння.









